您现在的位置是:首页 > 行业发展
miRNA技术应用研究|梧桐论道
智慧创新站
2025-04-22【行业发展】287人已围观
简介本篇文章选自梧桐树资本大健康团队王东东的《miRNA技术应用研究》。从六大层面全面分析miRNA技术应用行业当前市场环境与竞争格局。以下为文章目录:一、报告背景及结论二、RNA相关技术发展及应用三、MicroRNA(miRNA)相关技术应用进展四、miRNA相关公司五、国内核酸药物公司投融资情况六、...
本篇文章选自梧桐树资本大健康团队王东东的《miRNA技术应用研究》。从六大层面全面分析miRNA技术应用行业当前市场环境与竞争格局。以下为文章目录:
一、报告背景及结论
二、RNA相关技术发展及应用
三、MicroRNA(miRNA)相关技术应用进展
四、miRNA相关公司
五、国内核酸药物公司投融资情况
六、报告总结
01
报告背景及结论1.报告背景
公司在2020年10月份行研分享中,对RNA技术应用有了较为系统的研究。在报告“RNA相关技术发展及应用研究(赵玥)”中,对RNA技术发展进程、市场发展状况、RNA药物和技术、产业规模、行业政策、国内外主要RNA技术公司等情况做了详细研究,本篇报告为上次报告的续篇,着重介绍RNA技术中miRNA的相关技术和应用进展。
2.报告结论
核酸药物成为生物医药增长最快的细分领域。核酸药物主要包括反义核酸(ASO)、小干扰RNA(siRNA)、微小RNA(miRNA)、小激活RNA(saRNA)、信使RNA(mRNA)等。相较核酸ASO、RNAi和mRNA药物,miRNA药物的开发并不顺利,目前还没有miRNA药物获批上市,进展最快的到临床II期。miRNA可同时靶向多个mRNA靶标,但这也造成其成药特异性的问题,这也阻碍了miRNA药物开发的进程。
miRNA广泛参与调控细胞分化、增殖、凋亡、器官形成、个体发育等基本生命活动的阶段,miRNA既有调控作用,也可以作为很多疾病的标记物。研究中发现多种疾病的发生与miRNA异常表达有关,如肿瘤、肝炎、心血管疾病等。因此,miRNA一旦突破技术瓶颈,有着巨大应用潜力。全球看,miRNA前沿及临床研究一直处于热点状态,近期在心衰、糖尿病等领域也有不错的临床研究表现。国内张辰宇教授团队在miRNA领域的研究与产业化进展中处于领先水平,有望在miRNA药物领域实现创新性的突破。
02
RNA相关技术发展及应用(一)RNA概述和分类
核糖核酸(缩写为RNA,即RibonucleicAcid),存在于生物细胞以及部分病毒、类病毒中的遗传信息载体。RNA由核糖核苷酸经磷酸二酯键缩合而成长链状分子。RNA的碱基主要有4种,即A(腺嘌呤)、G(鸟嘌呤)、C(胞嘧啶)、U(尿嘧啶),其中,U(尿嘧啶)取代了DNA中的T(胸腺嘧啶)。核糖核酸在体内的作用主要是引导蛋白质的合成。
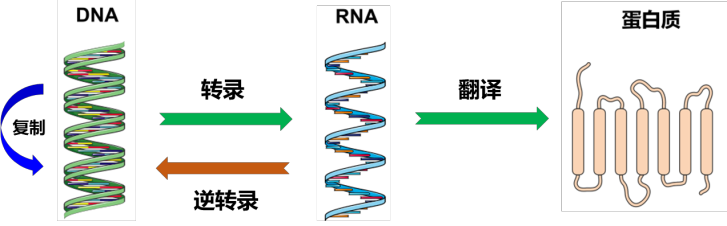
人类很多疾病的发生都与蛋白质结构、功能和数目变化密切相关,而人体内蛋白质合成均遵循中心法则。中心法则是指遗传信息从DNA传递给RNA,再从RNA传递给蛋白质的转录和翻译过程,以及遗传信息从DNA传递给DNA的复制过程。
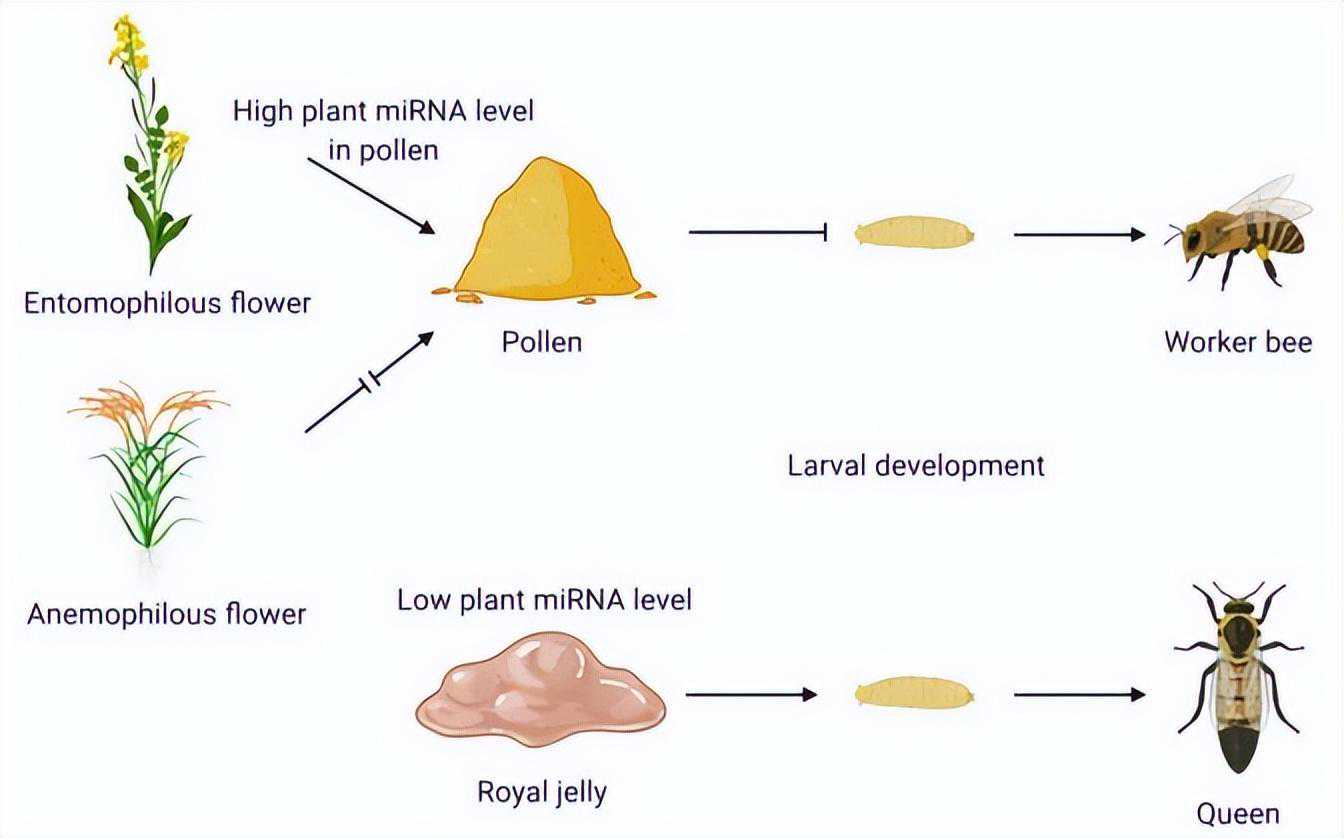
图:遗传信息的传递
核酸在生命活动中发挥着重要作用。核酸存在所有的生命体中,被认为是遗传信息的载体,用于转录、翻译为蛋白质,因此核酸是生物的最基本组成物质和生物学研究的基础物质;随着分子生物学的发展,人们发现有些DNA/RNA并不被转录/翻译为蛋白质,但他们依然对生命活动发挥着重要的调控作用,如DNA中的启动子、增强子,RNA中的核酶、微小RNA(miRNA)、小干扰RNA(siRNA)、小激活RNA(saRNA)等。
RNA根据功能可以分为转运RNA(tRNA)、信使RNA(mRNA)、核糖体RNA
(rRNA);根据是否参与遗传信息传递,又可分为编码RNA(mRNA)和非编码RNA(rRNA,tRNA,snRNA,snoRNA、microRNA、siRNA、piRNA等)。

图:RNA的分类及作用
(二)核酸药物发展概述
鉴于核酸在生命活动中发挥的重要作用,以及对不同种类核酸作用机制的揭示,人们开始尝试在核酸水平进行药物的设计,即为核酸药物。
1.核酸药物优势
核酸药物有望成为继小分子化药和抗体药物后的第三大类型药物。与传统的小分子化药和抗体类药物在蛋白质层面发挥药理作用不同,核酸药物是在基因转录和翻译过程中发挥作用,而核酸与互补序列结合的基础是碱基互补配对原则,因此核酸药物不具有部分靶点对小分子化药和抗体类药物不可成药的限制;而且多项技术的发展改善了核酸药物发展过程中遇到的问题,因此核酸药物被认为拥有较大的发展前景:
(1)候选靶点丰富
小分子和抗体药物均是通过与靶点蛋白结合发挥治疗作用。根据NatureReviewsDrugDiscovery的报道,在人类基因编码的超过20000个蛋白质中,可成药的蛋白仅有3000个,其中仅有700个蛋白质相对应的治疗药物被成功研发出来。
小核酸类药物是基于碱基互补配对原理,通过干扰翻译过程实现对基因表达的调控,无需与靶点蛋白质直接结合。因此,理论上任何由特定基因错误表达引起的疾病都可以通过小核酸药物进行治疗,这为小核酸药物的开发提供了丰富的候选靶点,使其突破了传统小分子化药和抗体类药物面临的限制。
(2)研发周期短
DNA测序技术的发展和成熟使得疾病相关的基因序列信息能够快速、准确地获取,而在知道靶基因的序列之后,即可进行小核酸药物的序列设计,大大缩短了药物开发的时间。以此次新冠疫情中Moderna公司mRNA疫苗的前期开发过程为例,COVID-19的核酸序列于2020年1月11日公布,Moderna在1月13日即完成mRNA疫苗序列的研究工作,2月7日完成首批样品制备,3月3日开始I期临床,3月16日即完成了首例患者给药,其前期开发速度远高于传统的疫苗。
(3)药效持久
整体而言,小核酸药物的有效作用时间比传统的小分子和蛋白药物更长。以siRNA药物为例,当靶标mRNA被降解后,RNA诱导的沉默复合体(RISC)可以循环工作,参与下一轮靶标mRNA的降解。因此,小核酸药物可在细胞内实现较长时间的药效作用,降低给药频率,提高患者治疗的依从性。较长的作用周期使得小核酸药物在糖尿病、心血管疾病等慢性病领域具有竞争优势。
(4)特异性强
传统的小分子和抗体药物与靶点的结合是结构驱动的,具有相似结构的蛋白质将影响药物的特异性。而小核酸药物与靶标的结合是序列驱动的,通过碱基互补配对识别特定目标序列,具有最小的或至少可预测的脱靶效应。因此,小核酸药物也具有相对更高的特异性。
(5)临床开发成功率高
小核酸药物以明确的疾病相关的核酸序列为目标,其针对性的设计避免了研发过程的盲目性,使得研究结果的确定性更强,临床开发的成功率也更高。
图:核酸药物优势
2.核酸药物种类及应用进展
核酸药物主要包括反义核酸(ASO)、小干扰RNA(siRNA)、微小RNA(miRNA)、小激活RNA(saRNA)、信使RNA(mRNA)、适配体(aptamer)、核酶(ribozyme)、抗体核酸偶联药物(ARC)等。目前全球共有17款核酸药物获批上市,包括9款ASO药物、5款siRNA药物以及2款mRNA疫苗(新冠疫苗)、1款aptamer药物,约80%的产品是2015年以后上市。
图:已上市核酸药物汇总
2022年6月13日,FDA批准了Alnylam开发的Amvuttra(vutrisiran),这是一款皮下注射给药的RNAi疗法,每三月注射一次,用于治疗成人遗传性转甲状腺素介导(hATTR)淀粉样变性的多发性神经病。
2020年12月,FDA先后批准了辉瑞/BioNtech和Moderna的两款mRNA新冠疫苗紧急使用,此后这两款产品在美国和欧盟不断的扩展适用人群及加强针适应症。2021年两款产品全球销售收入高达587亿美元。
据Insight数据库显示,当前,全球核酸新药进入临床管线的共有近397个,其中已经取得商业化成功的ASO疗法,是当前临床研发数量最多的核酸药物,共有137款,约占34%,其次为mRNA疫苗、siRNA等药物类型。同时,全球核酸药物涉及的疾病领域分布广泛,主要集中在肿瘤、感染性疾病、内分泌和代谢系统疾病等领域。从研发管线看,全球核酸药物约有5.2%进入了临床Ⅲ期,而进入临床Ⅰ期(含I/II期)和Ⅱ期,分别占27%和15%;大多数集中在临床前阶段,占比47%。
国内核酸药物研发目前尚处于起步阶段,研发管线主要以海外药企在国内开展临床为主,部分国内药企也通过自主研发或合作引进的方式占得一席之地,包括圣诺医药Sirnaomics(2257.HK)、瑞博生物、斯微生物、艾博生物等。
图:核酸药物在国内临床及上市情况
3.核酸药物开发关键技术
外源的核酸药物从进入体内到发挥药效作用需要克服多个难题:(1)稳定性问题,易被快速排出至体外或被体内的核酸酶降解;(2)免疫原性问题,会激活人体免疫系统的反应;(3)组织靶向问题,会在许多非药物活性部位的组织中积累,并产生毒性;(4)细胞摄取问题,核酸药物分子结构较大、亲水性高,且带有负电荷,穿透细胞膜的难度较高;(5)内体逃逸问题(osomeescape),核酸分子进入细胞后需要从内体中逃逸进入细胞质才能发挥作用。化学修饰和递送系统是解决上述问题的关键策略。
(1)化学修饰
对于小核酸药物进行化学修饰可以达到两个主要效果:首先,化学修饰可减弱生物体先天免疫机制对RNA药物的免疫反应,降低药物的免疫原性;其次,可增强RNA药物抵抗内源性内切酶和外切酶降解的能力,提高RNA的稳定性,延长药物半衰期。根据不同的修饰位点,目前常用的核苷酸化学修饰技术包括磷酸骨架修饰、核糖修饰、核糖五元环改造、碱基修饰、核苷酸链末端改造等。
(2)递送系统
化学修饰能够在一定程度上解决小核酸药物稳定性和免疫原性的问题,延长药物的半衰期,但仅依靠化学修饰的核酸药物在血液循环中还是容易被迅速降解、不易于在靶组织中积累、且不易有效地穿过靶细胞膜到达位于细胞质中的作用位点。因此需要借助递送系统的力量。当前主流核心递送技术包括脂质纳米颗粒(LNP)、脂质多聚复合物(LPP)、聚合物纳米颗粒(PNP)和GalNac技术。
图:核酸药物主要递送系统
脂质纳米颗粒(LipidNanoparticle,LNP)已在核酸药物中成功应用,也是目前小核酸药物领域研究最多的递送系统之一。
PNP是由人工合成的分枝状的组氨酸和赖氨酸的多肽共聚物(HKP)。在水溶液中,HKP多肽分子中的赖氨酸的氨基与核酸分子中的磷酸基通过离子键相互作用而结合(还有分子间的疏水键等其他相互作用)自组装形成一定大小的纳米颗粒。
GalNAc(N-乙酰半乳糖胺)是现阶段最常用也是最成功的配体类递送系统。在临床试验阶段的小核酸药物中,约有三分之一管线采用了多价GalNAc递送系统。
此外,外泌体递送技术以及多肽偶联技术等新的递送技术平台也在不断取得突破中。
外泌体是由细胞分泌的一种细胞外膜状脂质囊泡,作为天然内源性转运载体,细胞跨膜摄取效率高,不存在内体逃逸问题,无免疫源性问题,具有穿过血脑屏障等优势。可包载小分子、核酸、蛋白质、抗体、酶、细胞因子等,并针对特定的细胞类型和组织,可以精确地递送有效载荷,不激活先天或后天免疫系统,解决重复给药问题。CODIAK公司研发的外泌体载siRNA和反义核酸药物目前已经有进入二期临床的品种,Evox在2020年分别与武田制药(Takeda)和礼来公司(EliLillyandCo.)达成了9亿和12亿美元的合作协议,用于开发治疗罕见病和神经系统疾病的RNA药物。
图:外泌体递送核酸药物
国内方面,2021年3月29日,南京大学的张辰宇团队在CellResearch杂志发表了题为Invivoself-assembledsmallRNAasanewgenerationofRNAitherapeutics的论文,报道了一种利用合成生物学理念设计的基因环路实现siRNA体内高效递送的新技术。另外,2021年9月,深圳科兴药业有限公司与东南大学签署《关于共建细胞外囊泡递药技术产业化联合创新实验室的合作协议书》,推动国内外泌体载药技术向产业化的发展,联创实验室将获得稳定可靠的商业化规模的生产工艺和质量控制方法,并开发外泌体载药-递送-释放技术。
多肽具有分子量小、免疫原性低、特异性好、肾排泄等特点,兼具大分子与小分子的优势。多肽与小核酸偶联的多肽偶联物(PDC)也在成为核酸药物企业积极布局的重点领域。Ionis与Bicycle合作建立ASO/peptideplatform,双方合作主要基于转铁蛋白受体(TfR1),2021年7月30日,Alnylam与PeptiDream达成22亿美元合作协议,开发多肽-siRNA偶联药物。
图:全球多肽核酸偶联物情况
03
MicroRNA(miRNA)相关技术应用进展(一)MicroRNA简介
miRNA即微小RNA(microRNA),为单链RNA,通常15-25个核苷酸的长度,miRNA本身不编码蛋白质,但其可以与靶mRNA互补结合,调节其靶mRNA的翻
译过程。目前已经发现约2,000种miRNA,一个miRNA可以调节上百个mRNA的翻译,miRNA可以调节细胞的分化、增殖等过程,研究中发现多种疾病的发生与miRNA异常表达有关,如肿瘤、肝炎、心血管疾病等,因此通过miRNA也可开发针对这些疾病的药物。
MicroRNA的合成始于RNA聚合酶Ⅱ的转录过程:
编码miRNA的基因首先在细胞核内转录生成初级miRNA(pri-miRNA);随后,pri-miRNA将被RNaseIII家族酶Drosha和细胞核蛋白DGCR8的复合物切割,形成长度大约70-100nt、具有发夹结构的前体miRNA分子(pre-miRNA);pre-miRNA在核输出蛋白exportin-5的作用下被转运到细胞质,然后被另一个RNaseIII家族酶Dicer和TRBP的复合物进一步切割,形成长度约19-23nt的成熟miRNA;miRNA具有和siRNA相同特征的末端,随后其引导链将被加载到Argonaute蛋白上以形成RISC复合体,并介导靶mRNA降解,抑制其翻译。
图:miRNA的产生和作用机制
(二)miRNA治疗特点
miRNA和siRNA虽然机制相同但存在差异性。虽然也是形成RISC复合体,但与siRNA需要结合靶mRNA的3'和5'端21个核苷酸不同,miRNA仅与靶mRNA的5'端的2-8位核苷酸结合就能发挥作用。此外,与siRNA通过AGO2发挥作用不同,miRNA通过所有4种AGO蛋白调节其靶标。虽然它们有时会像siRNA一样导致mRNA裂解和降解,但miRNA的RISC主要通过抑制靶mRNA翻译和去腺苷酸化降解靶mRNA来实现基因沉默。
miRNA是人类细胞中天然存在的分子。与合成的化合物和ASO不同,miRNA具有处理和沉默下游靶标的机制,人类基因组中有超过70%的部分被转录成非编码RNA,选择广泛。
miRNA可以同时靶向多个基因。miRNA不需要以100%的互补性与其靶标完美结合,因此可以结合并抑制多种靶mRNA,从而形成一个庞大而复杂的调控网络。与仅影响单个靶基因的siRNA或ASO相比,miRNA可能会提高治疗效果,有利于解决疾病的异质性。然而,这种多基因靶向识别模式也同时增加了miRNA的脱靶概率。
miRNA作用机制具有多样性。与siRNA只能敲低基因表达不同,miRNA治疗可以上调或下调靶miRNA表达水平,调节方式更加多样化。
图:miRNA可以提高或降低目标基因表达水平
(三)miRNA与疾病的关系
1.miRNA与肿瘤
当细胞呈现出异常增长和凋亡功能丧失时,常常会导致肿瘤的形成。一些研究显示miRNA调节细胞的生长和凋亡。在很多恶性肿瘤中,已经鉴定出大约200种miRNAs有着不同程度的紊乱。与癌症相关的miRNA可分为两类:抑癌miRNA和致癌miRNA。在癌症发展过程中致癌miRNA(oncomiRs)主要表现为上调趋势,而肿瘤抑制性miRNA则为下调趋势。
癌症中oncomiRs的异常高表达通过直接与多个肿瘤抑制基因结合而下调这些mRNA的表达,从而导致癌细胞的生长、移动和转移。因此,从功能上抑制OncomiR是一种有效的癌症治疗策略。将与OncomiR互补的合成anti-miR引入癌细胞,可以阻止OncomiR与目标RNA的结合,从而抑制癌细胞的增殖和转移。
与OncomiR相反,肿瘤抑制性miRNA在肿瘤中的异常低表达通过逃避多种促癌基因表达的下调作为靶点,在肿瘤的发生和恶性进展中发挥作用。通过合成相关的肿瘤抑制性miRNA模拟物引入癌细胞的替代治疗被认为是一种治疗上合理的方法。
2.miRNA与神经系统疾病
虽然对miRNA如何调控神经系统发育成熟以及生理功能尚未完全清楚,但miRNA在神经系统的表达方式呈现高时序性、高保守性和高特异性等特征已被证实,因此探讨不同发育阶段、不同生理状态下miRNA功能至关重要。最近研究表明,miRNA不仅对发育早期胚胎干细胞存活和分化至关重要,而且在维持成熟神经元存活并使其发挥功能方面也起到重要作用。
图:miRNA与神经系统疾病
最近研究表明,循环的miRNA可作为神经退行性疾病的潜在的生物靶标。Martins等人采用微阵列技术对19位帕金森氏病(PD)患者和13位健康对照组的外周血单核细胞中的miRNA水平进行分析,鉴定出PD患者中有18种miRNAs存在差异表达,同时发现其中11种miRNAs在与PD相关的662个预测基因通路分析中具有过量表达。同时,Hebert等人采用RNA深度测序,分析健康对照组、阿兹海默症组、路易体痴呆组、海马硬化衰老组和额颞叶性痴呆五组中miRNA的表达情况,结果表明阿兹海默症和额颞叶性痴呆中miRNA-132的表达水平发生了较大变化。
Conaco等研究发现miR-124a表达也受到某些蛋白质调控。在非神经细胞中转录调节因子(REST)结合到miR-124a基因上从而抑制其表达,蛋白质表达呈非神经细胞表达模式,当REST抑制被解除后miR-124a表达增加从而调控蛋白质表达模式向神经方向转化。
图:miRNA与神经细胞调控
神经系统细胞种类繁多,功能较其他系统更为复杂,神经元、胶质细胞之间又通过轴突和树突形成一个个复杂的调控网络,精确掌控感觉、运动以及高级认知功能且神经系统需随外界环境变化及时调整自身功能。目前研究已经认为miRNA在神经系统发育和功能方面起到了精确的调控作用,一系列研究资料显示神经系统发育成熟和功能均受到miRNA精细调控,一旦调控出现紊乱必然导致疾病的发生发展。
3.miRNA与心血管疾病
心血管系统有着特别丰富的miRNAs资源,miRNAs在心血管疾病中充当多种多样的角色,或可反映心脏和血管对损伤的易感性,及哺乳动物对于持久心血管功能的依赖性。对心血管疾病小鼠模型和人类活检标本的miRNA分析揭示了miRNAs的标记模式可用于诊断多种心血管疾病,包括心力衰竭、心肌病、心肌梗死、动脉粥样硬化、局部缺血和血管生成。在小鼠中开展功能获得和丧失研究也验证了特异miRNAs在多种心血管疾病的病理生理学中的重要性。
miRNAs在心脏肥大、纤维化、心肌梗塞等心血管疾病也具有关键作用。Reddy等人发现在心肌细胞纤维化期间miR-21含量显著增加,进而导致心脏肥大。miR-143/145簇可靶向多种mRNA,这些mRNA编码蛋白可参与血管平滑肌细胞增殖和分化。在小鼠模型实验中发现,miR-143/145家族基因的下调会导致高血压和心力衰竭。慢性心脏应激反应会导致心肌产生病理性纤维化和肥大。
图:miRNA与心血管疾病
4.miRNA与其他疾病
microRNA还可作为糖尿病、HIV等疾病的治疗靶点。Poy发现胰腺特异的miR-375的过表达会抑制胰岛素的分泌,而抑制内源的miR-375的表达能增加胰岛素分泌,表明它可以作为治疗糖尿病的靶点。Kulkami等指出在HLA-C3'非翻译区域的变异影响着microRNA与其靶点的结合,进而影响HLA-C的表达及HIV的控制。Carpio等证实在HIV-1感染细胞中,由于HIV-1可以通过反式激活反应(trans-activationresponse,TAR)产生一种miRNA,这个miRNA可以改变宿主对于感染的响应,它从病毒的长末端重复序列开始限制病毒的复制,这个miRNA在保持病毒潜在的毒性方面发挥着重要作用。Cyckin/周期素依赖性蛋白激酶(Cdk)复合物对于病毒的复制很重要。由于microRNA这个调节机制的存在,Cdk抑制剂可以极大地增加反式激活反应中microRNA的数量,致使病毒长末端重复序列(LTR)转录的下调。
(四)miRNA在药物开发领域应用
1.miRNA数据库
生物信息学技术的飞速发展为miRNA的预测、发现以及功能鉴定提供了有效的帮助,目前已有多种生物信息学工具被开发并应用于miRNA生物发生的各个过程,为人们对miRNA的研究和应用提供帮助。
相关miRNA数据库总结如下:
2.miRNA药物开发
miRNA药物可分为拮抗剂和类似物。miRNA药物可分为两类:miRNA的拮抗剂(miRNAantagonist)以及miRNA类似物(miRNAmimics)。miRNA拮抗剂可以与miRNA以碱基互补配对原则结合并通过RISC对miRNA进行降解,以抑制miRNA的功能。miRNA类似物与人体内miRNA功能类似,将其导入病理细胞可使其恢复正常的生理功能。
目前尚未有miRNA药物获批,但已有一些miRNA药物的研发进入临床试验阶段。
图:miRNA药物开发情况
Miravirsen是最早进入到临床研究阶段的miRNA药物之一,采用锁核苷酸(LNA)技术的一段15nt长度反义RNA链,可同miR-122的5’端互补治疗HCV感染。后者对宿主的侵染过程严重依赖肝脏中丰度最高的miR-122。在啮齿类及非人灵长类动物模型中的临床前研究表明,Miravirsen展现出良好的肝脏输送效率、胆固醇积累量降低及HCV滴度减小,并据此于2009年启动Ⅰ期临床试验。Ⅰ期临床结果同在非人灵长类动物模型中的结论一致,推动了Ⅱa期临床试验的开展。该项Ⅱa期研究在7个国际中心展开,研究人员评估了Miravirsen用于36例慢性HCV1型感染患者的安全性和有效性。试验表明Miravirsen用于慢性HCV1型感染患者表现出长期剂量依赖性地减少HCVRNA水平的效应,且未出现病毒抵抗性。
图:miRNA药物用于治疗丙肝
miRNA药物只有10个项目进入临床,其中3项已经终止,2项暂停,5项还在临床开发,只有3项进入临床2期,没有项目进入3期临床。miRNA则作用成百上千个基因,很难做到特异性基因沉默,因而会产生不可预期的副作用。未来只有解决特异性作用的问题,miRNA药物或许才能够真正应用于临床。
在肿瘤治疗领域,进展最快的miRNA类似物为MRX34(MirnaTherapeutics),后者包裹于名称为NOV40的脂质载体中。NOV40粒子的优势在于低pH环境下,如肿瘤细胞的微环境,外周会携带正电荷,从而可以粘附于肿瘤细胞上。在小鼠模型中,研究人员观测到了MRX34纳米颗粒在肿瘤组织中的富集及显著的肿瘤组织缩小。2013年,MRX34进入了一项多中心的Ⅰ期临床试验,用于原发性肝癌,小细胞肺癌,淋巴瘤,黑色素瘤,多发性骨髓瘤或肾细胞癌患者的治疗。该试验包括剂量递增研究,每周2次给药或每天5次给药,MRX34通过静脉注射的方式给药。2016年,该项研究招募了99位肝癌、非小细胞肺癌及胰腺癌患者受试。尽管取得一定疗效,但由于免疫相关的负面事件(发生了5例严重的治疗相关副作用,4例发生死亡),该临床项目被终止。
RG-101是由RegulusTherapeutics开发的anti-miR-122药物,1期获得成功,可显著降低患者体内病毒滴度。对患者体内病毒数量反弹情况的长期监测表明,HVC水平低于定量范围。但是在2期临床试验中,由于黄疸病例的出现,该项临床试验被美国FDA暂停。
3.最新相关miRNA药物进展
①miRNA药物用于心衰治疗
德国制药公司CardiorPharmaceuticals基于德国汉诺威医学院ThomasThum教授的技术转化项目,开发miRNA药物用于心衰治疗。CDR132L是一种高度稳定的水溶性寡核苷酸ncRNA抑制剂,旨在阻断异常的micro-RNA-132水平,从而逆转细胞病理学并恢复心肌细胞的正常功能。在近期28名心衰患者的I期临床试验证实证实,CDR132L的人体安全性和耐受性良好,没有明显的毒性反应。同时,CDR132L可以使患者的心衰标志物NT-proBNP显著减少,心电图QRS波明显变窄,心肌纤维化标志物的改变也呈现出积极的趋势。
2021年8月25日,CardiorPharmaceuticals宣布完成6400万欧元(7600万美元)的B轮融资,本轮融资由InkefCapital领投,新投资者Fund+、Sunstone、HadeanVentures和Coparion等参投,现有投资者LSP、BioMedPartners、百时美施贵宝(BristolMyersSquibb)和High-TechGründerfonds跟投。
②miRNA药物用于糖尿病治疗
美国RosVivoTherapeutics开发的miRNA药物RSVI-301用于治疗糖尿病。胰腺β细胞和Cajal间质细胞(ICCs)中miR-10b-5p的失调可能是高血糖和胃肠运动障碍潜在的致病因素。RSVI-301是一款miRNA(微RNA)疗法,通过抑制致病基因翻译,恢复miR-10b-5p的水平,实现miR-10b-5p介导的KLF11-KIT途径进行调节作用,以治疗糖尿病。RosVivo进行了大量的动物模型实验,收集了RSVI-301与GLP-1受体激动剂相比的有效且令人信服的疗效数据。
图:RSV1-301与市场上的糖尿病药物利拉鲁肽/司美格鲁肽对比
2022年2月,采用miRNA技术的候选新药RSVI-301与礼来公司签署材料转让协议,礼来公司将审查和确认动物实验数据,并通过这份材料转让协议确保RSVI-301的潜力。
(五)miRNA作为诊断标志物
由于miRNA可以在体液中稳定存在,能在血浆、唾液、牛奶和脑脊液等体液中检测到,且易于通过微阵列、NGS和定量PCR进行检测,所以是生物标志物的理想候选者。
miRNA已被证明在癌症和其他疾病的发展和进展中起关键的调节作用。数以百计的miRNA在几乎所有种类的癌症中异常表达,不同的miRNA表达谱与肿瘤的发生、进展和治疗有关。miRNA可作为肿瘤抑制因子和癌变促进因子,调控细胞增生、凋亡、侵袭、转移和血管生成等。因此,监测miRNA标志物在肿瘤发生、发展中的作用,是其作为肿瘤诊断、预后标志物及治疗靶点的基础。
目前,国内获批用于癌症诊断或疗效监控的miRNA标志物产品主要集中在肝癌、结肠癌和胰腺癌。
图:获批用于癌症诊断或疗效监控的miRNA标志物产品
在淋巴瘤(DLBCL)患者的血清样本中miR-21、miR-155和miR-210表达上调。在乳腺癌(BC)患者血液中miR-195、miR-29a、miR-21、miR-16、miR-25、miR-222和miR-324-3p表达升高。miR-155在B细胞成熟中起作用,在B细胞和血浆中检测到miR-155升高可诊断为B-CLL。
急性髓系白血病(AML)患者血清中的miR-150和miR-342含量较高,且在完全缓解的AML患者中,miR-150和miR-342恢复到正常水平,表明这两种miRNA可以成为监测治疗效果的生物标志物。
除了用于疾病的预测外,miRNA还可作为药物治疗的预测生物标志物。miRNA的表达受药物影响,而且本身也可能影响药物的代谢和毒性,因此miRNA的表达也可用作药物功效的潜在生物标记,特别是循环miRNA,例如,miR-21的高表达和miR-200b的表达下调与对多种化疗药物的耐药性有关,可以作为患者对化疗反应的预测性替代生物标志物。
此外,目前有许多研究都证明了miRNA在创伤性脑损伤(traumaticbraininjury,TBI)、心血管疾病、阿尔茨海默病等多种疾病的诊断中都有一定的临床价值。
总体上,miRNA作为疾病诊断的标志物的临床应用还处于较早期的阶段,而RNA结构的多样性、核苷酸的修饰和不同、样本制备等技术难题,也需要更多的深入研究和临床验证。
(六)张辰宇教授miRNA前沿研究
1.细胞外miRNA
图:miRNA由细胞内到细胞外的认知过程
2.miRNA的跨界调控
2017年,南京大学生命科学院陈熹团队在PLOSGenetics杂志发表研究论文,研究发现蜂粮里的植物miRNA通过抑制蜜蜂幼蜂的卵巢和整体的生长发育,使之成为工蜂。而蜂王浆中不含有植物miRNA,因此吃到蜂王浆的幼蜂则发育为蜂王。
图:植物miRNA调控蜜蜂幼蜂生长发育
3.中草药中的miRNA调控
2014年,张辰宇团队在CellResearch发表研究论文,发现,金银花在作为中药汤剂时,即使经过长时间煮沸,仍然存在富集的完整序列的MIR2911,这是由于其序列中GC含量高,在高温下仍能保持稳定。在体外和体内试验中,MIR2911能够靶向多种流感病毒基因。小鼠实验则表明,饲喂金银花汤剂的小鼠血液和肺中MIR2911显著升高,且MIR2911抑制了各种甲流病毒(包括H1N1,H5N1和H7N9)在小鼠体内的复制,减轻了病毒感染引起的体重减轻,并降低了小鼠死亡率。
图:植物种MIR2911可以抑制病毒
2019年6月,张辰宇团队等在BioMaterials杂志发表论文,该研究设计并开发了一种基因工程生菜,以生物合成人工miRNA,以生菜的内源性miRNA生物发生机制特异性靶向乙肝病毒表面抗原基因(HBsAg)。口服生菜汤后,人造miRNA被吸收并传递到肝脏中,以抑制转基因小鼠中HBsAg的表达。
治疗15个月后,HBsAg的表达降低,转基因小鼠模型的肝损伤明显减轻,且未观察到毒理作用。由于工程植物生产干扰序列的有效性、无毒性且经济可行的优势,这种方法也可以拓展到丙型肝炎或其他传染疾病的治疗。
4.miRNA作为血清标志物
miRNA可在人类和动物的血清和血浆中稳定存在,成为所有血清miRNA生物标志物研究的基础。
图:miRNA作为疾病诊断的血清标志物
张辰宇教授团队在2015年,开发的国际上首个针对miRNA标志物的胰腺癌诊断试剂盒获得国家批准,对早期胰腺癌的检测准确率达87.6%。
图:命码生物公司胰腺癌诊断产品
5.合成生物学自组装外泌体递送技术
目前核酸药物递送策略的共同特征是在体外将siRNA与载体或配体预组装。然而,这些人工复合物经常受到诸如免疫相容性低、毒性高、循环稳定性不足和组织可及性受限的问题困扰。因此,开发安全、精确和有效的siRNA递送平台,对于下一代RNAi疗法至关重要。
合成生物学自组装外泌体递送技术原理:在体外合成包含病毒抗原模版和相关调控指令组件的基因环路,基因环路通过静脉、肌肉注射等方式递送到体内后,以哺乳动物自身的组织器官作为天然生物基盘,将外源siRNA的自我组装引导到分泌性外泌体中,并促进体内自组装siRNA的系统/靶向递送。
图:自组装外泌体递送技术原理
技术优势:
①人工设计的基因环路既是药物,又是载体。从而避免了传统递送方式带来的递送效率损失和安全性风险,内源性、生物相容性高无毒、无免疫原性;
②实现在同一环路上表达、组装并递送多个siRNA,同时抑制多个基因表达,从而使得可以针对不同疾病、不同患者的情况,针对性设计药物,实现真正的个体化治疗;
③可穿过生物屏障。
基于此技术,张教授创建了艾玛生物,注于小RNA核酸药物研发,管线主要包括对难治性实体瘤的治疗,例如胰腺癌等;对中枢神经系统疾病的治疗,例如亨廷顿症、帕金森病、脑胶质瘤;以及金银花中MIR2911的广谱抗病毒研究,这包括对新冠病毒的治疗作用。
图:艾玛生物主要研发管线
04
miRNA相关公司(一)RegulusTherapeutics
RegulusTherapeutics成立于2007年9月,总部位于美国加利福尼亚州,是一家致力于发现和开发以微RNA(microRNA)为靶标的创新药物研发公司。RegulusTherapeutics利用其寡核苷酸药物发现和研发平台,建立了microRNA药物研发线。其创新技术包括利用硫代磷酸酯骨架提高代谢稳定性,2’-O-甲氧基乙基(MOE)核苷调节安全性,以及高亲和力的双环修饰如限制型乙基(cEt)核苷创造出更强效的化合物。RegulusTherapeutics正在推进几个肾脏、肝脏和中枢神经系统疾病项目。主要候选产品包括治疗Alport综合征的RG-012、治疗常染色体显性多囊肾病的RGLS4326和治疗胶质母细胞瘤的RGLS5579。
Regulus针对遗传性肾炎的管线已进入临床II期阶段,针对常染色体显性多囊的管线已进入临床I期阶段。此外,公司还正在进行针对感染、肝脏疾病等领域的miRNA药物开发。
图:Regulus研发管线
2022年5月11日,美国FDA批准该公司在研新药RGLS8429临床(IND)申请,用于治疗常染色体显性多囊肾病(ADPKD)。RGLS8429是一种新型的下一代寡核苷酸,旨在抑制miR-17并优先靶向肾脏。从而使尿外泌体样囊泡中的PC1和PC2蛋白水平增加,逆转囊肿形成。2022年6月13日,RegulusTherapeutics公司宣布RGLS8429在单剂量爬坡I期临床试验中完成首例健康受试者给药。
RegulusTherapeutics目前在纳斯达克市值约为2350万美元。
(二)ViridianTherapeutics
MiragenTherapeutics公司三款主要候选产品,包括:
MRG-106——AntimiR-155,用于治疗弥漫性大B细胞淋巴瘤,目前处于临床II期;
MRG-110——miR-29mimic,在各种病理性纤维化病症中处于低水平,包括皮肤,心脏,肾,肝和肺纤维化,以及系统性硬化症,目前处于临床II期;
MRG-110——AntimiR-92,在内皮细胞中表达,并显示在心力衰竭,外周缺血和皮肤创伤的临床前模型中加速新血管的形成,目前处于临床I期;
ViridianTherapeutics目前在纳斯达克市值约为4亿美元。
(三)CardiorPharmaceuticals
CardiorPharmaceuticals是一家德国制药公司,成立于2016年。公司基于德国汉诺威医学院ThomasThum教授的技术转化项目,开发miRNA药物用于心衰治疗。CDR132L是一种高度稳定的水溶性寡核苷酸ncRNA抑制剂,旨在阻断异常的micro-RNA-132水平,从而逆转细胞病理学并恢复心肌细胞的正常功能。在28名心衰患者的I期临床试验证实证实,CDR132L的人体安全性和耐受性良好,没有明显的毒性反应。同时,CDR132L可以使患者的心衰标志物NT-proBNP显著减少,心电图QRS波明显变窄,心肌纤维化标志物的改变也呈现出积极的趋势。
2021年8月25日,CardiorPharmaceuticals宣布完成6400万欧元(7600万美元)的B轮融资,本轮融资由InkefCapital领投,新投资者Fund+、Sunstone、HadeanVentures和Coparion等参投,现有投资者LSP、BioMedPartners、百时美施贵宝(BristolMyersSquibb)和High-TechGründerfonds跟投。
(四)RosVivoTherapeutics
美国RosVivoTherapeutics是一家miRNA创新药物研发商,致力于开发利用miRNA(微小核糖核酸)技术治疗糖尿病、肥胖、非酒精性脂肪肝(NAFLD)、胃肠(GI)运动障碍和新冠肺炎的新药物产品。
RosVivoTherapeutics开发的miRNA药物RSVI-301用于治疗糖尿病。胰腺β细胞和Cajal间质细胞(ICCs)中miR-10b-5p的失调可能是高血糖和胃肠运动障碍潜在的致病因素。RSVI-301是一款miRNA(微RNA)疗法,通过抑制致病基因翻译,恢复miR-10b-5p的水平,实现miR-10b-5p介导的KLF11-KIT途径进行调节作用,以治疗糖尿病。RosVivo进行了大量的动物模型实验,收集了RSVI-301与GLP-1受体激动剂相比的有效且令人信服的疗效数据。
图:RSV1-301与市场上的糖尿病药物利拉鲁肽/司美格鲁肽对比
2022年2月,采用miRNA技术的候选新药RSVI-301与礼来公司签署材料转让协议,礼来公司将审查和确认动物实验数据,并通过这份材料转让协议确保RSVI-301的潜力。
(五)昆山彭济凯丰
2013年由彭长庚博士创立于江苏昆山小核酸研究基地。专注于研发miRNA(第三代小核酸)相关的小核酸新药、保健品和微RNA科研试剂。
自建了微核酸药库并筛选到一批原创性的治疗代谢类疾病和癌症等方面的潜在微小分子核酸新药,主要治疗糖尿病、肾病,在动物体内效果显著。公司申报生物技术类、新药发明专利18项,其中2项已获授权,另外公司已递交5项PCT申请。其中,可能填补市场空白的1.1类治疗糖尿病肾病的小核酸新药研发项目PJ150021于2018年获得国家重大新药创制科技重大专项立项支持,已先后2次接受制药巨头礼来的考察。
(六)西安荣清畅
西安荣清畅生物科技有限公司(简称“荣清畅”)成立于2017年10月。公司专注于miRNA技术产品开发及RNA药物研发,是一家以世界领先的miRNA生产专利技术为核心,以高表达携带功能性miRNA科研产品为主导,集研发、生产、销售和科研服务、检测于一体的高新技术企业。
(七)江苏命码生物
命码生物成立于2008年,是基于公司首席科学家张辰宇教授原创发现“细胞外小核酸稳定存在,并具有独特生物学功能”的科学规律,并在此基础上发展的基础研究、应用基础研究、转化研究及产业转化的生物医药高新科技企业。
公司开发了全球第一个基于血清miRNA的胰腺癌诊断试剂盒,2015年获证。基于血清miRNA的胰腺癌诊断试剂盒的成功开发,当前对疑难病如精神分裂症、抑郁症、阿尔茨海默症、埃博拉病毒和食管癌等传统无法检测的疾病都找到了分子标志物并做到早期检测,已开发出实验室试剂盒。
(八)骏实生物科技(上海)有限公司
骏实生物成立于2006年,是一家为医院、实验室提供专业体外诊断试剂和相关仪器研发、生产的高新技术企业。
公司拥有世界首个被批准上市的miRNA7™肝癌分子诊断产品。该产品是中国科学院院士、复旦大学附属中山医院院长樊嘉团队历经多年攻关,在肝癌患者的血浆中,筛选到由7个微小核糖核酸(microRNA)组成的早期肝癌诊断分子标记物,并在此基础上开发了检测试剂盒。2017年8月,获得CFDA的三类医疗器械注册证和器械生产许可证;2018年1月,正式在国内上市。
图:公司miRNA产品及检测流程
(九)深圳市晋百慧生物有限公司
公司创办于2013年,总部位于中国深圳,是一家专注于尖端体外诊断技术与前沿分子生物学研究的国家高新技术企业。
晋百慧生物研发的基于RNA-based生物路径技术的肠癌检测试剂(睿长太®),是国内首款获得三类医疗器械注册证的肠癌粪便检测试剂。
粪便样本中的miRNA具有良好的稳定性和检测可重复性。miR-92a是小分子编码RNA,属于人类13号染色体的miR-17-19基因簇,通过抑制PTEN、KLF4和下游p21基因促进结直肠癌细胞增殖和迁移。患有结直肠癌或息肉病变者粪便样本中miR-92a含量均较正常水平显著增高,可作为结直肠癌检测标志物。
图:公司产品信息
(十)深圳市展行生物有限公司
深圳市展行生物有限公司于2014年创立,公司产品聚焦microRNA癌症早期筛查及预后监测、心脑血管疾病的筛查、HIV空窗期检测及干细胞治疗等领域。
公司核心产品覆盖miRNA肿瘤及心脑血管疾病早期筛查、HIV空窗期超微量检测、干细胞疾病治疗与抗衰老等领域。展行生物秉承“知未病,智生活”的理念,致力于成为人类生命健康的守护者。展行microRNA肿瘤超早期筛查采用特异性加尾法,结合高灵敏度的qRT-PCR技术,对受检者血浆中与肿瘤相关的微量microRNA进行精准的pg级别检测,从而在癌症发生的超早期动态检测受检者的癌症的发生状况,进而采取科学有效的预防干预措施。目前展行MicroRNA肿瘤超早期筛查覆盖包括肺癌、肝癌、胃癌、食管癌、结直肠癌、乳腺癌、宫颈癌7种高发癌症。
图:公司产品套餐
05
国内核酸药物公司投融资情况图:国内核酸药物企业融资汇总表
06
报告总结在新冠mRNA疫苗的催动下,核酸药物成为生物医药增长最快的细分领域。小核酸药物全球市场规模从2016年0.1亿美元已增长至2021年32.5亿美元,年复合增长率高达217.8%。
目前的核酸药物中,ASO、RNAi和mRNA药物最为成功,目前这三类药物均已有相关产品上市。miRNA广泛参与调控细胞分化、增殖、凋亡、器官形成、个体发育等基本生命活动的阶段,miRNA既有调控作用,也可以作为很多疾病的标记物。
在药物应用领域,miRNA药物的开发并不顺利。miRNA药物只有10余个项目进入临床,其中3项已经终止,2项暂停,5项还在临床开发,只有3项进入临床2期,没有项目进入3期临床。miRNA则作用成百上千个基因,很难做到特异性基因沉默,因而会产生不可预期的副作用。miRNA药物特异性作用的问题还没有完全解决。
国内南京大学张辰宇教授在miRNA领域取得了系列进展,原创发现“细胞外小核酸稳定存在,并具有独特生物学功能”的科学规律,开发了全球第一个基于血清miRNA的胰腺癌诊断试剂盒。并基于胞外miRNA理论基础,发现了细胞外囊泡封装的miRNA具有基于RNAi的基因治疗的潜力、基因改造食用植物以生物合成miRNA作为药物具有直接通过食用进行基因治疗的潜力,并开发了抗肿瘤,抗感染、精神/神经性疾病等多条miRNA药物产品管线。有望在miRNA药物领域实现创新性的突破。
-END-
很赞哦!(160)
相关文章
- 保障国家能源安全 科技创新为深海油气勘探开发添“利器”
- 强瑞技术:无法就原重组方案达成一致,将变更投资方案,拟5085万元投资三烨科技等公司
- 几十吨“白银”竟然是锌,银行被坑8000万!
- 中兴通讯申请通信网络负荷调整方法专利,能够提高通信小区的负荷调整效果
- 福州市150辆机动车闯红灯违法行为曝光
- 杭州童尚科技有限公司新零售 用新的经济模式在添新的活力
- 迅游科技“内斗”总裁袁旭遭罢免 4年累亏逾21亿“光速大师”收入归零
- 【国企动态】菏泽市土发集团与中勘天成(北京)科技有限公司召开合作交流座谈会
- 80万年薪+200万安家费!天津科技大学诚邀全球英才加盟
- (上接C45版)深圳市振邦智能科技股份有限公司首次公开发行股票招股意向书摘要(下转C47版)